Saúde
Anvisa altera condições para autorização do uso emergencial de vacinas contra a Covid-19
Isso acontece após Pfizer desistir da solicitação à agência brasileira por conta de demora nos processos exigidos
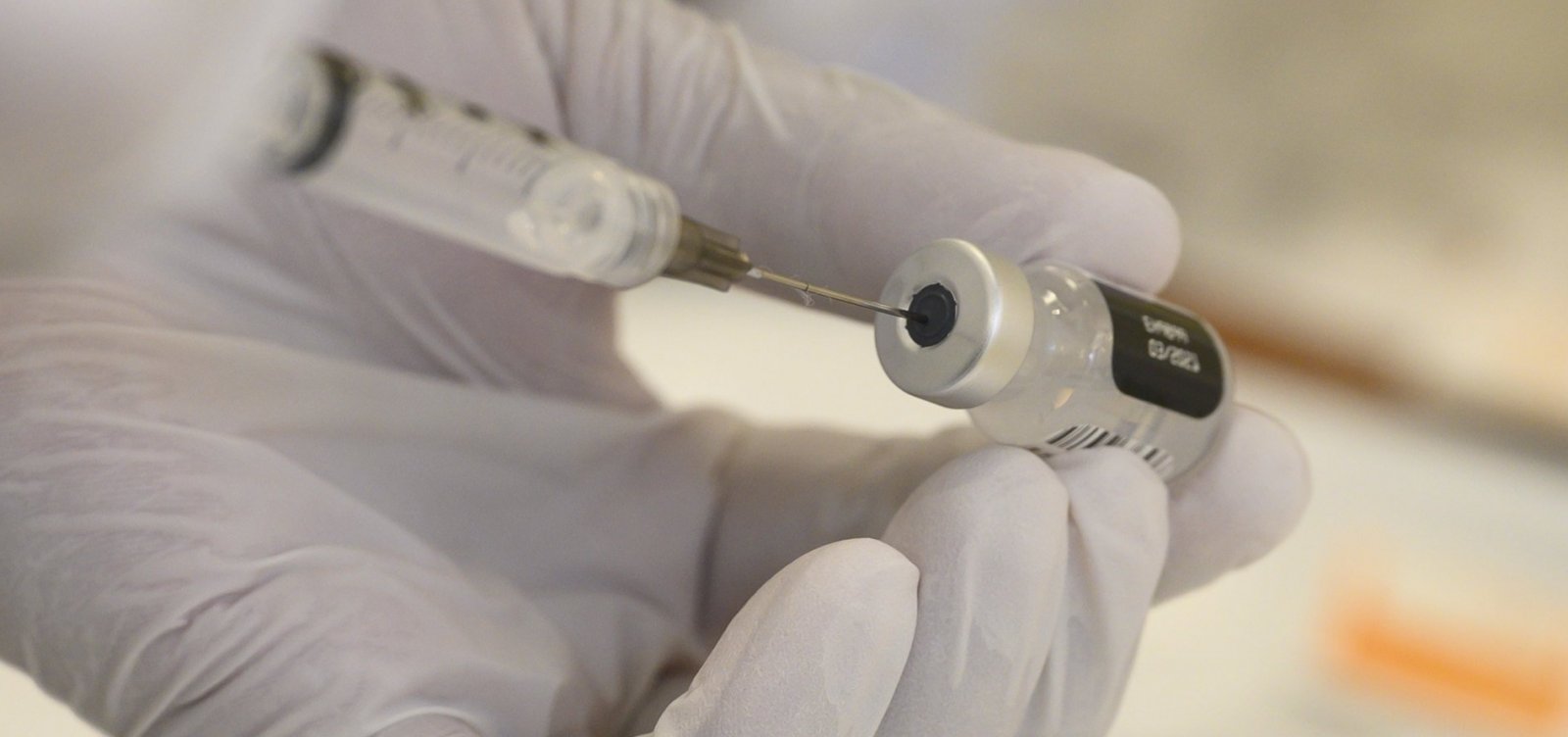
Foto: DoD photo by Lisa Ferdinando
A Agência Nacional de Vigilância Sanitária (Anvisa) modificou ontem (29), os critérios utilizados para avaliação e aprovação do uso emergencial de vacinas contra o coronavírus. Isso acontece após a empresa farmacêutica Pfizer desistir da solicitação à Anvisa para uso emergencial da vacina fabricada por ela no Brasil.
O imunizantes produzido pela Pfizer/BioNTech têm 95% de eficácia e já foram autorizados e distribuídos na União Europeia, nos Estados Unidos e em outros países. No Brasil, porém, o laboratório percebeu que a avaliação dos critérios exigidos pela agência demorariam muito, por isso, avaliaram que não seria interessante fazer o pedido para uso emergencial, apenas do registro definitivo (que demora mais).
Algumas das alterações feitas pela Anvisa foram a retirada da imposição da existência de um cronograma de disponibilização ao país, da exigência da informação da quantidade exata de doses disponíveis e sugere, como em outros países, um formulário de termo de consentimento a ser assinado pelo paciente que receber a vacina em uso emergencial.
📲 Clique aqui para fazer parte do novo canal da Metropole no WhatsApp.