Saúde
Anvisa deve decidir nas próximas semanas sobre registro de rivais do Ozempic no Brasil
Pedidos de medicamentos à base de semaglutida, incluindo produto da EMS, estão na fase final de análise; expectativa é de aumento da concorrência e possível redução de preços após fim da patente
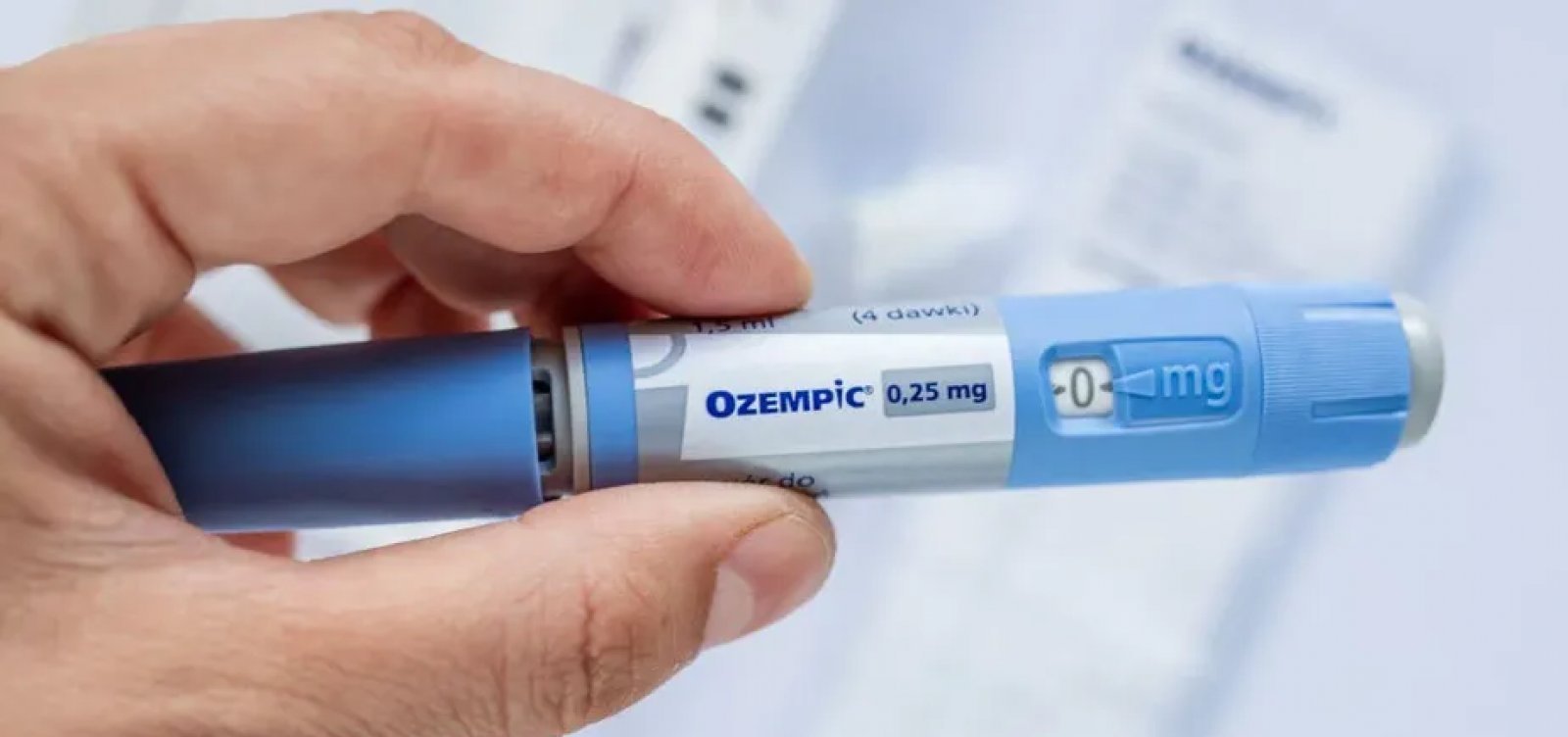
Foto: Divulgação
A Anvisa (Agência Nacional de Vigilância Sanitária) informou que deve se manifestar nas próximas semanas sobre o pedido de registro de dois medicamentos à base de semaglutida que pretendem concorrer com o Ozempic e o Wegovy, ambos fabricados pela Novo Nordisk. A patente da substância vence em 20 de março, mas ainda não há concorrentes aprovados no Brasil.
Segundo a agência reguladora, os dois pedidos estão na fase final de revisão interna. Um deles é da EMS, que já comercializa canetas emagrecedoras de geração anterior à base de liraglutida, concorrentes do Saxenda e do Victoza. O outro processo foi protocolado inicialmente pela Momenta, do grupo Eurofarma, e posteriormente transferido para a Ávita Care.
A Eurofarma já atua nesse segmento após firmar, em 2025, parceria com a Novo Nordisk para distribuição de marcas de semaglutida. Paralelamente, a Anvisa informou que rejeitou, em dezembro, um pedido de registro de medicamento com liraglutida apresentado pela Megalabs.
Além da semaglutida, o mercado conta com a tirzepatida, princípio ativo do Mounjaro, fabricado pela Eli Lilly, cuja patente é válida até 2036. Recentemente, a Câmara dos Deputados aprovou regime de urgência para um projeto que propõe a quebra de patente de produtos com tirzepatida, medida que enfrenta resistência da indústria e do governo federal.
Atualmente, há 14 pedidos de registro de produtos com semaglutida e sete com liraglutida em análise na Anvisa. Nenhum deles se enquadra como genérico, categoria que exige preço ao menos 35% inferior ao do medicamento de referência, mas o setor avalia que a entrada de novos concorrentes pode reduzir os valores no mercado.
Em 2025, o governo federal solicitou prioridade na análise de 20 pedidos relacionados a medicamentos emagrecedores. A Anvisa afirma, porém, que estabeleceu limite para processos acelerados, a fim de evitar prejuízos a outras demandas, e justificou a medida com o risco de desabastecimento e com a priorização de etapas de fabricação nacional.
📲 Clique aqui para fazer parte do novo canal da Metropole no WhatsApp.