Saúde
Estudo da USP aponta que vacina contra herpes-zóster é segura para pacientes com doenças reumáticas
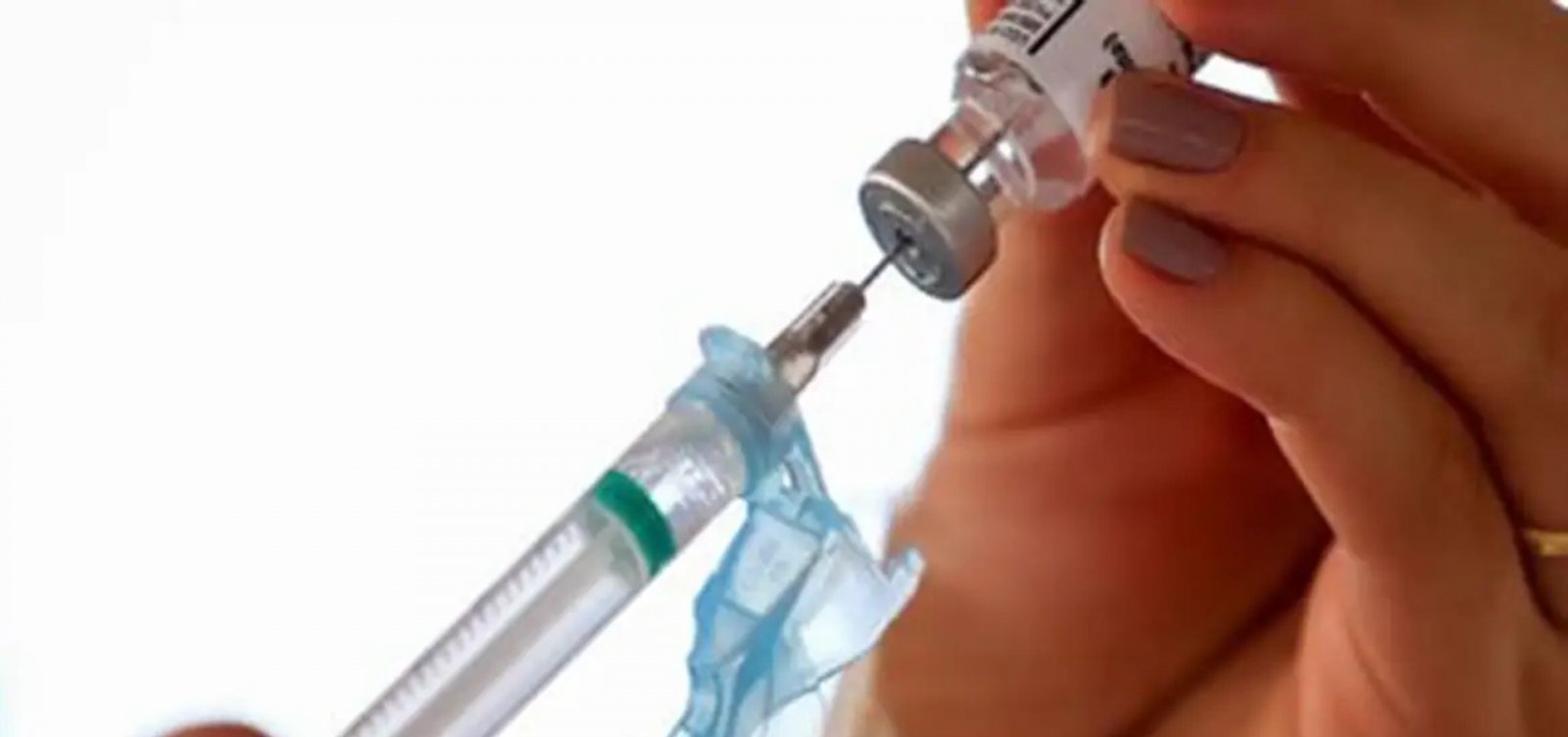
Uso em larga escala e registro definitivo só deve vir a partir de 15 de janeiro
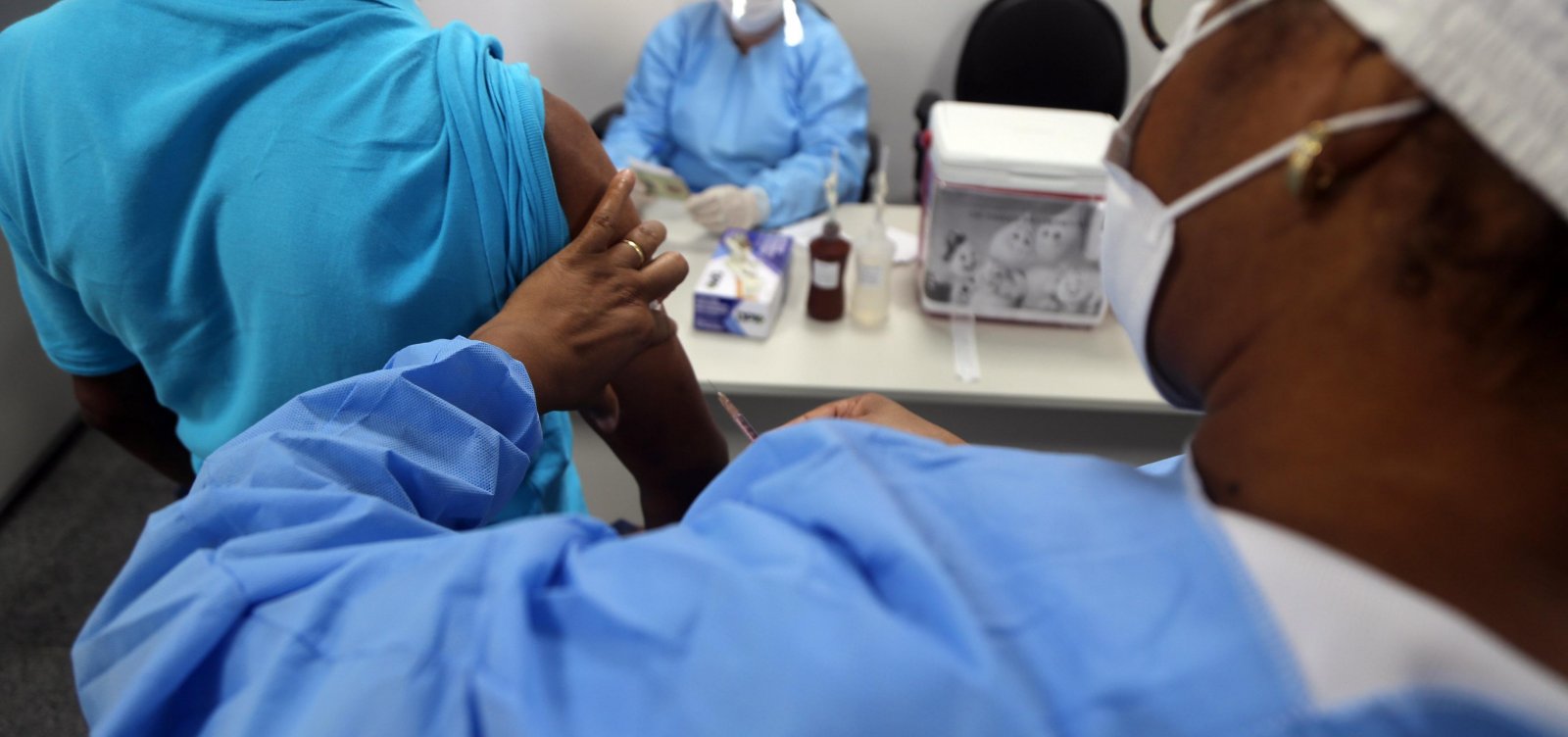
Foto: Bruno Concha/PMS/Secom
A Fundação Oswaldo Cruz (Fiocruz) informou hoje (4) à Agência Nacional de Vigilância Sanitária (Anvisa) que pedirá autorização para uso emergencial da vacina desenvolvida pela Universidade de Oxford e a farmacêutica AstraZeneca contra o novo coronavírus até sexta-feira (8). A informação foi publicada pelo site UOL, que apurou que o aviso foi feito por diretores da fundação em reunião com técnicos da Anvisa que cuidam dos protocolos de vacinação. A solicitação para uso emergencial permite aplicação de doses em grupos de risco. Oficialmente, além de pedir o uso emergencial até sexta-feira, a fundação comunicou que deve solicitar o registro definitivo no dia 15 de janeiro, possibilitando o uso em larga escala. No país, nenhum laboratório fez pedido à Anvisa para começar a vacinação.
A reunião teve participação da presidente da Fiocruz, Nísia Trindade Lima, diretores da fundação e técnicos da Anvisa. No encontro, técnicos da agência reguladora pediram que a Fiocruz prove que a vacina importada da Índia é semelhante àquela aplicada no Reino Unido.
No último sábado (2), a Anvisa informou que foi aprovado o pedido para que a Fiocruz importe da Índia 2 milhões de doses já prontas da vacina desenvolvida pela Universidade de Oxford e a farmacêutica AstraZeneca. Mas para que sejam aplicadas, além de provar que são semelhantes às do Reino Unido, é necessário também a autorização para uso emergencial.
Segundo a Anvisa, a previsão é que após o pedido de uso emergencial, em até dez dias o corpo técnico se manifeste pelo uso ou não do fármaco.
📲 Clique aqui para fazer parte do novo canal da Metropole no WhatsApp.